在生命科学研究的严谨道路上,一个长期存在的“隐形杀手”正悄然损耗着无数课题的经费、时间与心血——那便是潜藏于SPF兔体内的巴氏杆菌病。
长期以来,国内供应市场陷入一个令人无奈的困局:大量标称“SPF级”的实验兔,在送达客户实验室后的短期内,频频出现大面积鼻炎、肺炎、乃至急性死亡等典型症状。这不仅导致动物模型在实验关键期意外折损,更使得整个研究项目的数据可靠性蒙上阴影,造成的损失远超动物本身的价值。
此顽疾何以成为行业通病?主流供应商又为何难以从根本上予以杜绝?
本文将深入剖析这一困局背后的深层技术与管理原因,并系统阐述我司如何通过种群、人员物资管控和饲养环境等方面,真正实现SPF兔群的巴氏杆菌阴性化,为您的关键实验提供坚实、纯净、稳定的动物模型基础。
我们深知,每一只实验兔都承载着探索的期望。破解此困局,是我们对科学严谨性的承诺,也是对您宝贵科研投入的负责。
核心困境:兔多杀性巴斯德杆菌难以防护的原因

1.高携带率与潜伏感染
- “隐形”携带者:这是最核心的难点。在兔群中,有非常高的比例(可达50%-90%) 的兔子是无症状携带者。它们看起来完全健康,但细菌却长期潜伏在它们的上呼吸道(如鼻腔)、扁桃体或中耳。
- ·间歇性排菌:这些携带者会间歇性地通过打喷嚏、鼻腔分泌物等将细菌排到环境中,成为移动的、难以识别的传染源。你无法通过肉眼观察找出所有带菌兔。
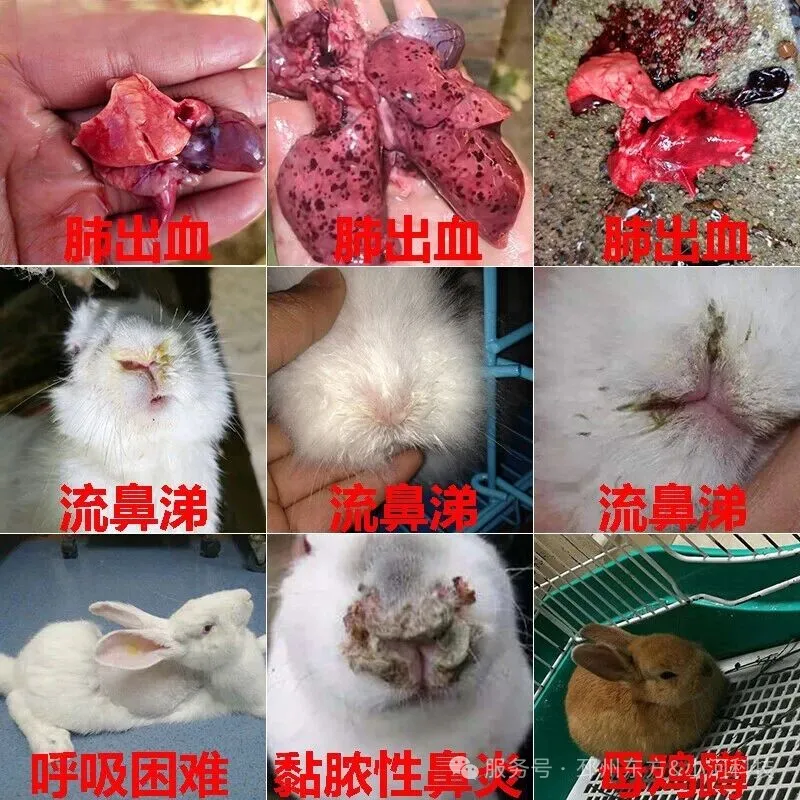
2.传播途径机器简单直接
- 气溶胶传播:一个喷嚏或咳嗽,就能将含有大量细菌的飞沫散布到空气中,附近的兔子通过呼吸即可感染。
- 接触传播:通过直接接触(如互相理毛、交配、打斗)或间接接触(如被污染的饮水器、食盆、笼壁、操作人员的手套和衣服)传播。
- 这种高效的传播方式使得一旦有排菌者存在,病原体在兔群中蔓延几乎难以阻止。
3.应激触发机制
巴斯德杆菌在携带者体内可以与宿主“和平共处”,直到应激因素出现,打破这种平衡,导致疾病爆发。这些应激源在实验或饲养环境中几乎不可避免:
- 环境应激:运输、温度/湿度骤变、通风不良、氨气浓度过高。
- 生理应激:断奶、怀孕、分娩、营养不良。
- 实验应激:更换笼具、保定、采血、手术、免疫抑制实验等。
这意味着,即使一个兔群平时保持“临床健康”,一次看似普通的实验操作或环境波动,就可能引爆一场巴斯德杆菌病。
4.定植牢固,难以清除
- 免疫逃逸:巴斯德杆菌能够形成生物被膜,这是一种附着于黏膜表面的细菌群落,对抗生素和宿主免疫系统的清除有极强的抵抗力。
- 病灶隐匿:细菌可以藏匿在解剖学上难以触及的部位,如中耳腔和鼻窦深处。全身性给药的抗生素很难在这些部位达到足以彻底清除细菌的有效浓度。
5.治疗与根除困难
- 抗生素只能控制症状,难以根除:抗生素治疗可以缓解急性感染的临床症状(如停止流脓鼻涕),但一旦停药或遇到新的应激,疾病很可能复发,因为细菌并未被完全清除。
- 无有效商业化疫苗:目前尚无广泛有效、能提供完全保护的商品化疫苗用于兔群。菌株血清型多样且免疫原性复杂,使得疫苗研发困难。
6.检测方法的局限性
- “检测阴性”不等于“未感染”:常用的鼻拭子PCR或细菌培养方法,如果恰逢携带者处于排菌间歇期,或者细菌藏匿在中耳等深处,就可能得到假阴性结果。
- 血清学检测的局限:血清学检测(检测抗体)只能说明兔子曾经接触过该病原,无法区分是当前活跃感染还是既往感染,也无法识别出无症状携带者。

总结:防护的“不可能三角”
防护多杀性巴斯德杆菌的困难,可以概括为面对一个“不可能三角”的挑战:
1. 无处不在的传染源:无法完全识别的、高比例的隐形携带者。
2. 无法切断的传播途径:简单高效的空气和接触传播,在群养环境中几乎无法彻底阻断。
3. 一触即发的易感状态:各种难以避免的应激因素,随时可将携带状态转为发病状态。
因此,对于实验兔群而言,最有效且经济的策略并非在已感染的兔群中进行“治疗”和“防护”,而是采取“净化”和“排除”的顶层设计:
- 建立和维持SPF级兔群:通过子宫切除术或胚胎移植等严格手段,建立无特定病原的原始种群,并在绝对屏障设施中繁育和饲养。这是唯一能从根本上解决问题的方法。
- 严格的生物安全体系:对于SPF群,通过严格的检疫、人员物资管控和环境管理,坚决将病原拒之门外。
结论:
多杀性巴斯德杆菌之所以难以防护,是因为它在兔群中完美地扮演了一个“潜伏的特工”角色——隐藏深、传播易、触发快、清除难。传统的“边养边防”模式效果有限,真正的突破口在于从源头上建立一个无此病原的清净种群。




